Гриппол® Плюс – тривалентная вакцина для профилактики гриппа с доказанной эффективностью и безопасностью
Вакцинация от гриппа: здоровье привитых под иммунным зонтиком
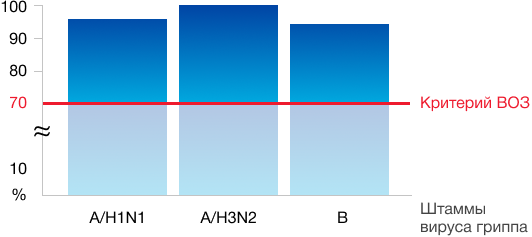
Иммуногенность вакцины Гриппол® плюс соответствует требованиям ВОЗ
Уровень серопротекции, %
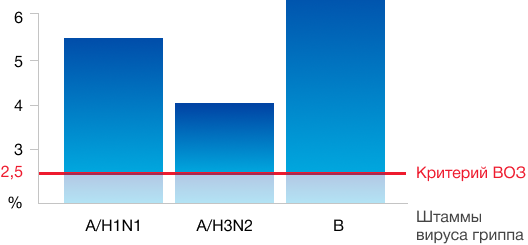
Кратность нарастания титров антител
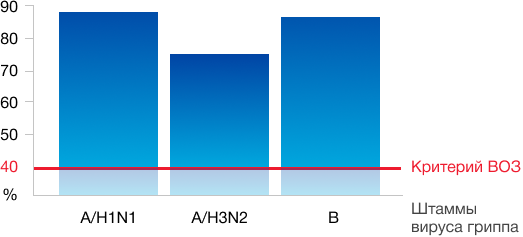
Уровень сероконверсии, %
- Гриппол® плюс обеспечивает эффективную защиту ко всем трём антигенам актуальных штаммов вируса гриппа у 95-100% вакцинируемых
- Более чем у 70% вакцинированных отмечено четырёхкратное увеличение титра антител
- После вакцинации титр защитных антител увеличивается в 4 и более раз
Выраженный иммунный ответ формируется уже на 8-12 день после вакцинации и сохраняется до 12 месяцев
Таблица 1. Клинические исследования вакцины Гриппол® плюс.
| Дизайн, популяция, количество | Оцениваемые параметры | Результаты |
|---|---|---|
| Рандомизированное двойное слепое плацебо контролируемое Здоровые добровольцы 18-55 лет1, n=61 |
Безопасность Иммуногенность вакцин, содержащих по 5 и по 10 мкг гемагглютинина каждого штамма Группы: Гриппол® Гриппол плюс (по 5 мкг на штамм) Гриппол плюс (по 10 мкг на штамм |
Безопасность
Слабые нормальные общие вакцинальные реакции отмечены у 6.9% вакцинированных (недомогание, субфебрильная температура). Ни у одного привитого не отмечено сильных общих вакцинальных реакций или поствакцинальных осложнений. Местные реакции (болезненность в месте введения в течение 30-60 минут) отмечены у 14.8% привитых. |
|
Рандомизированное двойное слепое контролируемое, Здоровые добровольцы 18-27 лет, n=300 |
Доля лиц с защитным титром для штаммов A / H1 N1; A / H3 N2 и В:
Гриппол: 98%, 85%, 70%, соответственно Гриппол плюс по 5 мкг: 95%, 84%, 76%, соответственно Гриппол плюс по 10 мкг: 94%, 90%, 88% Доля лиц с 4-х-кратным приростом:Гриппол: 97.5%, 78%, 63% Гриппол плюс по 5 мкг: 89.1%, 73.5%, 79.6% Гриппол плюс по 10 мкг: 95.5%, 88; 90.1% для штаммов A/H1N1; A/H3N2 и В, соответственно. Кратность приростаВарьировала в диапазоне от 6.7 до 31.6. Выбрана доза по 5 мкг на каждый штамм |
|
|
Рандомизированное двойное слепое контролируемое, сравнительное в параллельных группах2. Дети 3-17 лет N=153 |
Безопасность Иммуногенность 2 Группы: 1 - Гриппол® плюс 2 - Вакцина сравнения |
Безопасность:
Частота общих и местных реакций – 5,6% Местных реакций не отмечено. Число общих реакций: головная боль -1, недомогание – 2, боль в животе – 1 Иммуногенность:Доля лиц с 4-кратным приростом к штаммам A/H1N1; A/H3N2 и В титров: 96%, 87% и 100%, соответственно у исходно серонегативных и 100%, 71.4% и 40%, соответственно у исходно серопозитивных. Кратность нарастания титров19.9, 18.3, 6.0, соответственно у исходно серонегативных и 5.3, 6.5, 2.8 у исходно серопозитивных. Доля лиц с защитным титромк штаммам A/H1N1; A/H3N2 и В: к штаммам A/H1N1; A/H3N2 и В: |
|
Рандомизированное двойное слепое контролируемое, сравнительное в параллельных группах3 Дети 6 – 35 месяцев, n=140 |
Сравнение безопасности и иммуногенности при использовании двух режимов вакцинации: Группа 1 - двукратно дозой 0,5 мл с интервалом 21-28 недель Группа 2 - двукратно дозой 0,25 мл с интервалом 21-28 недель |
Безопасность:
Ни один из режимов не влиял на клинические параметры крови Местные реакции (боль, покраснение, припухлость) после первой и второй вакцинации варьируется в диапазоне: 3.1% – 7.4% Общие реакции (головная боль, недомогание, нарушение аппетита, нарушение сна, потливость, насморк, кашель) варьируется в диапазоне 1.5% - 14.5%. Все они были кратковременными, не требовали медикаментозной коррекции. |
|
Открытое проспективное типа «случай-контроль» рандомизированное с ослеплением в основной группе по конечным точкам Пожилые люди от 60 лет и старше4, n=721 |
Безопасность
Иммуногенность спустя 1 месяц и 6 мес Профилактическая эффективность |
Безопасность:
Местные реакции (боль, покраснение, зуд, уплотнение в месте введения) зарегистрированы у 16,6% вакцинированных. Проходили в течение 3 дней самостоятельно. Общие реакции отмечали у 22% вакцинированных. Наиболее частая – головная боль (14%-16%), боль в суставах (2.5%–3.4%), субфебрильная температура (до 37.5) – 2.5%. Все реакции были кратковременными и проходили самостоятельно. ИммуногенностьСпустя месяц после вакцинации: Доля лиц с защитным титром: 67.4% - 80.0% Доля лиц с 4-кратным приростом: 39.0% - 68.9% Кратность прироста титров антител: 2.6 (для гриппа В) – 6.5 (для гриппа А) Спустя 6 месяцев после вакцинации: Доля лиц с защитным титром: 53.80% - 64.4% Доля лиц с 4-кратным приростом: 21.7% - 55.1% Кратность нарастания по сравнению с исходным уровнем: 1.8 (для гриппа В) -4.3 (для гриппаА) Профилактическая эффективность:Снижение заболеваемости ОРВИ и частоты эпизодов обострения основного хронического заболевания в группе привитых. |
|
Рандомизированное открытое контролируемое, с ослеплением по конечным точкам в параллельных группах5 Дети 3-17 лет с аллергическими заболеваниями, n=160: 106 с аллергическими заболеваниями (пищевая аллергия, БА, поллиноз), 54 - здоровых ребенка |
Безопасность Иммуногенность Вакцины: Гриппол® плюс Инфлювак |
Безопасность
Обе вакцины показали благоприятный профиль безопасности в отношении общих и местных реакций. Достоверных различий в безопасности и переносимости двух вакцин не выявлено. ИммуногенностьСпустя 1 месяц кратность прироста в штаммам A/H1N1, A/H3N2 и в составили соответственно: 2.1 – 4.7, 2.5-3.7 и 1.3-2.7 у детей с аллергическими заболеваниями и 2.8-3.5, 1.8-2.1 и 1.4-1.6 у здоровых детей. Доля лиц с 4-кратным приростом среди исходно серонегативных составила 45.5%-52.9% в группе вакцинированных Грипполом® плюс и 50.0%-63.6% в группе вакцинированных Инфлюваком. Доля лиц с защитным титром составила 69.2%-80.8% в группе Гриппол плюс и 64.7%-94.1% в группе Инфлювак. Достоверных различий в иммуногенности вакцин не выявлено |
Таблица 2. Результаты эпидемиологических пост-регистрационных когортных исследований вакцины Гриппол® плюс
| Сезон, город | Контингент, число участников | Заболеваемость гриппом на 1000 с учетом серологического подтверждения | Общая заболеваемость ОРВИ на 1000 в течение всего сезона | Другие результаты | ||
|---|---|---|---|---|---|---|
| Привитые | Не привитые | Привитые | Не привитые | |||
|
2008-2009 Санкт-Петербург, Россия6 |
Школьники 7-17 лет, n=2768 (5 школ) |
69,2 | 172,1 | 214,8 | 301,4 |
1. Эффективность вакцины, рассчитанная с учетом серологического подтверждения диагноза «грипп», при среднем охвате исследуемых коллективов прививками 36.1% составила 59.8% 2. Ни у одного привитого не отмечено выраженных общих или местных поствакцинальных реакций и осложнений 3. Вакцинация препаратом Гриппол® плюс способствовала уменьшению количества осложнений у заболевших: в группе непривитых гриппи ОРЗ протекали с осложнениями в 2,5 раза чаще, чем у привитых |
|
2008-2009 Подольск, Россия7 |
Школьники 7-15 лет, n=3203 (9 школ) |
75 | 16 | 399,3 | 546,8 |
1. Эффективность вакцины, рассчитанная с учетом серологического подтверждения диагноза «грипп», составила 78,7% [72.4% — 90.9%] 2. В школах с охватом прививок ≥ 60% учащихся общая заболеваемость ОРВИ (случаи на 1000 человек) была на 40% ниже, чем в школах с охватом прививок £ 60% 3. В школах с охватом ≥ 60% отмечено в 3,4 раза меньшее количество «часто болеющих» детей по сравнению со школами с низкой «иммунной прослойкой» (3.1% и 10.6% детей, соответственно, р < 0,01) |
| Витебск, Гродно, Минск, Республика Беларусь8 |
Школьники 6-17 лет, n=5391 (6 школ) |
39 | 113 | 240 | 557 |
4. Эффективность вакцины в отношении гриппа составила 66,2% 5. У вакцинированных детей достоверно меньшее число случаев повторного заболевания и количество осложнений (гайморит, бронхит, пневмония) по сравнению с непривитыми. |
|
Взрослые с 18 лет и старше, n=6917 (3 предприятия) |
15 | 31 | 97 | 187 |
6. Эффективность вакцины в отношении гриппа у взрослых составила 50,3% 7. При общем низком уровне заболеваемости во всех 3 городах, риск заболевания (ОР) вакцинированных был достоверно ниже (p < 0,05), чем непривитых: ОР [95% CI]: Гродно: 0,63 [0,53 – 0,75]; Витебск: 0,26 [0,15 – 0,43]; Минск: 0,72 [0,60 – 0,86]; |
|
- беременные9, 10, 11 и новорожденные от вакцинированных беременных12, 13;
- пожилые люди в возрасте 60 лет и старше с болезнями системы кровообращения14, 15;
- дети и взрослые с бронхиальной астмой и другими хроническими обструктивными заболеваниями дыхательных путей16, 17, 18;
-
дети с сахарным диабетом19.
Таблица 3. Сравнение эффективности вакцин Гриппол Плюс, Инфлювак и Ваксигрип на 28 день после вакцинации.
| Параметр иммуногенности вакцины | Требование CPMP * | Результаты исследования | ||
|---|---|---|---|---|
| Гриппол плюс | Инфлювак | Ваксигрип | ||
| Штамм A/H1N1 | ||||
| Фактор сероконверсии | Более 2,5 | 7,20 | 7,57 | 8,06 |
| Уровень сероконверсии | Более 40% | 93,2% | 94,6% | 94,4% |
| Уровень серопротекции | Более 70% | 95,0% | 95,0% | 96,0% |
| Штамм A/H3N2 | ||||
| Фактор сероконверсии | Более 2,5 | 3,78 | 4,59 | 4,32 |
| Уровень сероконверсии | Более 40% | 67,4% | 77,8% | 92,5% |
| Уровень серопротекции | Более 70% | 90,9% | 90,0% | 96,0% |
| Штамм B | ||||
| Фактор сероконверсии | Более 2,5 | 2,70 | 2,50 | 3,27 |
| Уровень сероконверсии | Более 40% | 71,4% | 90,0% | 93,8 |
| Уровень серопротекции | Более 70% | 99,0% | 100,0% | 100,0% |
|
* - для каждого штамма по крайней мере один показатель должен отвечать указанным требованиям. |
||||